1. Атом Резерфорда – Бора
Примеры решения задач
| Сайт: | Система электронного и дистанционного обучения СВФУ |
| Курс: | Физика атома и ядра. Слепцов И.А., Слепцов А.А. |
| Книга: | 1. Атом Резерфорда – Бора |
| Напечатано:: | Гость |
| Дата: | Tuesday, 23 July 2024, 08:31 |
Примеры решения задач
Задача №1.
Определить скорость, с которой электрон движется по первой боровской орбите в атоме водорода.
Задача №2.
Частица массы движется в центрально-симметричном силовом поле \( \vec{F} \)=-kr(k>0). Применяя теорию Бора выразить через циклическую частоту ω, с которой колебалась бы частица под действием \( \vec{F} \):
а) возможные радиусы rn круговых орбит частицы
б) возможные значения En полной энергии частицы.
Задача №3.
Вычислите в электрон-вольтах (эВ) потенциальную энергию водорода в состоянии, которому в модели атома Бора соответствует радиус круговой орбиты, равный 0,53 Å.
Задача №4.
Чему равна частота фотона, испущенного при переходе водородоподобного атома Li++ из состояния n=5 в состояние m=4.
Задача №5.
Фотон с энергией 12,1 эВ, поглощенный атомом водорода, находящимся в основном состоянии привел атом в некоторое возбужденное состояние. Каково квантовое число этого состояния.
Задача №6.
У какого водородоподобного иона разность длин волн головных линий серий Бальмера и Лаймана равна 59,3 нм.
Задача №7.
Найти квантовое число n, соответствующее возбужденному состоянию водородоподобного иона He+, если при переходе в основное состояние этот ион испустил последовательно два фотона с длинами волн 108,5 и 30,4 нм.
Задача №1.
Определить скорость, с которой электрон движется по первой боровской орбите в атоме водорода.
|
Дано: H |
Решение: |
|---|---|
|
Найти: v1=? |
Запишем систему уравнений
\( m\frac{v^2}{r_n}=k\frac{Ze^2}{r^2_n} \), |
(1) |
mvrn=nћ. |
(2) |
Z - зарядовое число атомного ядра, e - элементарный заряд, rn - радиус
\( v_n=k\frac{e^2}{\hbar}\cdot\frac{Z}{n} \). |
(3) |
Зарядовое число Z атома водорода равно единице, следовательно, окончательно имеем
\( v_1=k\frac{e^2}{\hbar} \). |
(4) |
Задача №2.
Частица массы движется в центрально-симметричном силовом поле \( \vec{F} \)=-kr(k>0). Применяя теорию Бора выразить через циклическую частоту ω, с которой колебалась бы частица под действием \( \vec{F} \):
а) возможные радиусы rn круговых орбит частицы
б) возможные значения En полной энергии частицы.
|
Дано: \( \vec{F}=-k\vec{r} \) mvr=nћ |
Решение: |
|---|---|
|
Найти: rn=? En=? |
a)
mvrn=nћ. |
(1) |
v=ωrn. |
(2) |
Поставим (2) в (1)
\( m \omega{r^2_n }=n\hbar \). |
(3) |
Отсюда следует
\( r_n=\sqrt{\frac{n\hbar}{m\omega}} \). |
(4) |
б) Полная энергия частицы равна
E=T+U. |
(5) |
Выразим кинетическую энергию T через частоту ω:
\( T=\frac{mv^2}{2}=\frac{m}{2}\cdot{\omega}^2\cdot\frac{n\hbar}{m\omega}=\frac{n\hbar\omega}{2} \). |
(6) |
Для нахождения потенциальной энергии U воспользуемся определением
\( F=-\frac{dU}{dr} \). |
(7) |
По условию задачи имеем
F=-kr. |
(8) |
Применяя равенства (7) и (8), запишем уравнение
dU=krdr. |
(9) |
Здесь учтено, что \( \vec{F} \uparrow \uparrow\vec{r} \). Частота ω квазиупругих колебаний определяется формулой
\( \omega=\sqrt\frac{k}{m} \). |
(10) |
Если учесть (10), то дифференциал dU потенциальной энергии примет вид
dU=mω2rdr. |
(11) |
Интегрируем обе части равенства (11):
\( U=m{\omega}^2 \int{rdr}=\frac{m{\omega}^2r^2}{2} \). |
(12) |
И, наконец, учтя (4), найдем
\( U=\frac{n\hbar\omega}{2} \). |
(13) |
Из формул (6) и (13) следует, что полная энергия частицы равна
En=nћω. |
(14) |
Задача №3.
Вычислите в электрон-вольтах (эВ) потенциальную энергию водорода в состоянии, которому в модели атома Бора соответствует радиус круговой орбиты, равный 0,53 Å.
|
Дано: r=0,53 |
Решение: |
|---|---|
|
Найти: U=? |
Потенциальная энергия электростатического взаимодействия электрона с ядром равна
\( U=-k\frac{Ze^2}{r} \). |
(1) |
В системе СИ e=1,602·10-19Кл, k=9·109м/Ф, 1 Å=1010м, 1 эВ=1,6·10-19Дж.
\( U=\frac{{(1,602\cdot10^{-19})}^2}{0,53\cdot10^{-10}\cdot1,6\cdot10^{-19}}=-27,2 \) эВ. |
Задача №4.
Чему равна частота фотона, испущенного при переходе водородоподобного атома Li++ из состояния n=5 в состояние m=4.
|
Дано: n=5 m=4 |
Решение: 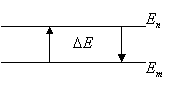 |
|---|---|
|
Найти: ω=? |
Обобщенная формула Бальмера - Ридберга для водородоподобного атома на шкале имеет вид
\( \omega==R'\left(\frac{1}{m^2-n^2}\right)Z^2 \), |
(1) |
где R′ - константа Ридберга на шкале частот, целые числа m и n означают номер серии и номер линии в ней соответственно. В случае атомного ядра лития Z=3. R′=2,07·1016c-1. Расчет:
\( \omega=2,07\cdot10^{16}\left(\frac{1}{16}-\frac{1}{25}\right)=4,2 \) c-1. |
Задача №5.
Фотон с энергией 12,1 эВ, поглощенный атомом водорода, находящимся в основном состоянии привел атом в некоторое возбужденное состояние. Каково квантовое число этого состояния.
|
Дано: E=12,1 эВ |
Решение: 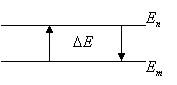 |
|---|---|
|
Найти: n=? |
Энергия перехода равна
ΔE=En-Em=|Em-En|. |
(1) |
Энергия Ef фотона, излучаемого (или поглощаемого) при квантовом переходе между уровнями En и Em равна
Ef =ΔE. |
(2) |
При этом частота перехода определяется формулой Бальмера - Ридберга
\( \omega=R'\left(\frac{1}{m^2}-\frac{1}{n^2}\right) \). |
(3) |
Следовательно, энергия фотона равна
\( E_f=\hbar\omega={\hbar}R'\left(\frac{1}{m^2}-\frac{1}{n^2}\right) \). |
(4) |
По условию задачи Em есть основное состояние, то есть m=1. Отсюда следует, что
\( n=\frac{1}{\sqrt{1-E_f/{\hbar}R'}} \). |
(5) |
Расчет:
\( n=\frac{1}{\sqrt{1-12,1/13,6}}=3,02 \). |
(6) |
Здесь мы учли, что потенциал ионизации атома водорода равен ћR′=13,6 эВ. Ответ: n=3.
Задача №6.
У какого водородоподобного иона разность длин волн головных линий серий Бальмера и Лаймана равна 59,3 нм.
|
Дано: Δλ=59,3 нм |
Решение: |
|---|---|
|
Найти: Z=? |
Для водородоподобного атома формула Бальмера - Ридберга на шкале волновых чисел имеет вид
\( \tilde{v}=\frac{1}{\lambda}=R\left(\frac{1}{m^2}-\frac{1}{n^2}\right)Z^2 \), |
(1) |
где константа Ридберга R=1,097·107м-1. С учетом номеров серий и головных линий в них запишем следующие равенства:
\( \frac{1}{\lambda_Л}=R\left(\frac{1}{1^2}-\frac{1}{2^2}\right)Z^2=\frac{3RZ^2}{4} \) для серии Лаймана, |
(2а) |
\( \frac{1}{\lambda_Б}=R\left(\frac{1}{2^2}-\frac{1}{3^2}\right)Z^2=\frac{5RZ^2}{36} \) для серии Бальмера. |
(2б) |
Используя условие задачи и соотношения (2), найдем уравнение для нахождения Z
\( \frac{36}{5RZ^2}-\frac{4}{3RZ^2}=59,3\cdot10^{-9} \). |
(3) |
Отсюда имеем
\( Z= \pm\sqrt{\frac{9,9435\cdot10^7}{R}} \approx \pm3,0106 \). |
Порядковым номером элемента будет положительное целое число, ближайшее к найденному значению, то есть Z=3. Такой номер принадлежит литию, следовательно, символ иона Li++.
Задача №7.
Найти квантовое число n, соответствующее возбужденному состоянию водородоподобного иона He+, если при переходе в основное состояние этот ион испустил последовательно два фотона с длинами волн 108,5 и 30,4 нм.
|
Дано: He+ λ1=108,5 нм λ2=30,4 нм |
Решение: 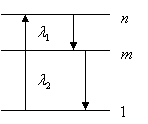 |
|---|---|
|
Найти: n=? |
Используя формулу Бальмера - Ридберга для водородоподобного атома, запишем два равенства
\( \frac{1}{{\lambda}_1}=r\left(\frac{1}{m^2}-\frac{1}{n^2}\right)Z^2 \), |
(1) |
\( \frac{1}{{\lambda}_2}=r\left(\frac{1}{1^2}-\frac{1}{m^2}\right)Z^2 \). |
(2) |
Сложим равенства и получим
\( \frac{{\lambda}_1+{\lambda}_2}{RZ^2{\lambda}_1{\lambda}_2}=1-\frac{1}{n^2} \). |
(3) |
Отсюда находим
\( n=\frac{1}{\sqrt{1-({\lambda}_1+{\lambda}_2)/(RZ^2{\lambda}_1{\lambda}_2)}} \). |
(4) |
Расчет:
\( n=\sqrt{1-138,9\cdot{10}^{-9}/(1,097\cdot{10}^7\cdot{4}\cdot108,5\cdot10^{-9}\cdot30,4\cdot10^{-9})} \approx4,9809 \). |
Следовательно, n=5.